Gas idealen legea. Gasen nahasketak
Gas idealen edo perfektuen legea adierazten duen ekuazioa, gasen banakako legeetan oinarritua dago eta portaera ideala izaten badute, behintzat, gasaren masaren eta P, V eta T aldagaiaren arteko lotura laburbiltzen du ekuazio horrek. Gasen nahasketa batean, biek egiten duten presio totala, egoera berean gas bakoitza bakarrik egongo balitz egingo lukeen presioaren batuketa da.
Gas idealen legea
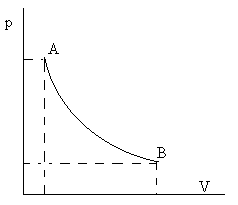
Gas baten egoera lau magnitude lotzerakoan zehazten da: bolumena (V), tenperatura (T),presioa (P) eta gas kantitatea moletan adierazia (n). Erlazio horiek zehazten dituzten legeak honako hauek dira:Boyle Legea:

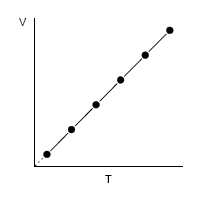
Charles Legea:
V = konstantea × T (P eta n zehatzetan)
Avogadro Legea:
V = konstantea × n (P eta T zehatzetan)
Proportzionalitate horiek konbinatuz erlazioa lortuko dugu:

Konstantea R sinboloak adierazten du, eta hala gas idealen edo perfektuen legea lor dezakegu:
PV = nRT
R konstateari gas idealen edo gasen konstante unibertsala deitzen zaio. Balio bera du gas guztientzat, eta bolumen molarrari eta gas baten egoera arrunta (0 ºC eta atm 1) deitzen zaienei esker kalkula daiteke.
Portaera ideala duen edozein gasen bolumen molarra 22,4 litrotan zehaztu da esperimentu gisa. Horrenbestez:

Gas idealen edo perfektuen ekuazioari esker, gasen bolumenak erlazionatu daitezke beti, presioa eta gasen tenperatura edozein delarik ere.
Gasen nahasketa: Dalton legea
Euren artean erreakzionatzen ez duten gasen nahasketa batean, molekula bakoitza independienteki mugitzen da, modu berdintsu batean edo erabat bakanduta egongo balira bezala.
Nahasketa horretan, gas bakoitza uniformeki banatzen da libre dagoen eremu osoan zehar, beste gasen bat bertan egongo ez balitz bezala. Molekulek gasa dagoen ontziko hormetan egiten duten presioa, beste edozein gas egongo ez balitz bezala egingo lukeen presioaren berdina da.
1803an, Daltonek (1766-1844) presio partzialen legea adierazi zuen: "gasen nahasketa batean, gasek egiten duten presio totala, gas bakoitza baldintza berdinetan egongo balitz egingo lukeen presioaren batuketa da".
A, B eta C gasak ontzi berean sartzen baditugu, nahasketa homogeneo bat osatzen dute. Gas bakoitzak, banaka, nahasketa batean egiten duen presioari presio partziala deitzen zaio.
Honela adierazten da presioen Dalton legea:
Pguztira = PA + PB + PC + ¿
Osagai bakoitzak, banaka, nahiz gasen nahasketak gas idealen edo perfektuen ekuazioa betetzen du, eta honako hau da:
Pguztira × V = (nA + nB + nC+ ¿) RT
Masaren, dentsitatearen eta gas baten masa molekularraren edo molarraren erlazioak
Gasen bolumen berdinek presio eta tenperatura baldintza beretan molekula kantitate bera dute. Baldintza horiek aldaketarik gabe mantenduz gero, gasen bolumen berdinen masak nahasketa hori osatzen duten molekulen masarekiko proportzionalak izan behar dute. Ondorengo ekuazioa betetzen da:

Gas baten presioa, bolumena eta tenperatura ezagutzen badira, masa molekularra, gasaren dentsitatea edo lagin baten masa zein den ondoriozta daiteke:

Gas idealen ekuazioan ordezkatuz gero:

Gasaren dentsitatea ere ezagutu daiteke honela: